MP Board 11th Chemistry Quarterly Exam 2025-26 Question Bank : DPI द्वारा जारी किए गए नवीनतम पाठ्यक्रम पर आधारित MP Board 11th Chemistry Quarterly Exam 2025-26 Question Bank अब उपलब्ध है! यह प्रश्न बैंक आपकी त्रैमासिक परीक्षा की तैयारी को पूर्णता प्रदान करने के लिए विशेष रूप से तैयार किया गया है। इसमें उन सभी अति-महत्वपूर्ण प्रश्नों का संकलन है, जिनके परीक्षा में आने की प्रबल संभावना है।
इस MP Board 11th Chemistry Quarterly Exam 2025-26 Question Bank से तैयारी करके आप न केवल अपने समय का सदुपयोग करेंगे, बल्कि यह सुनिश्चित करेंगे कि आप केवल सबसे प्रासंगिक सामग्री का ही अध्ययन करें। यह आपकी परीक्षा में शानदार प्रदर्शन करने की कुंजी है! अभी इसका उपयोग करें और अपनी सफलता की नींव रखें।

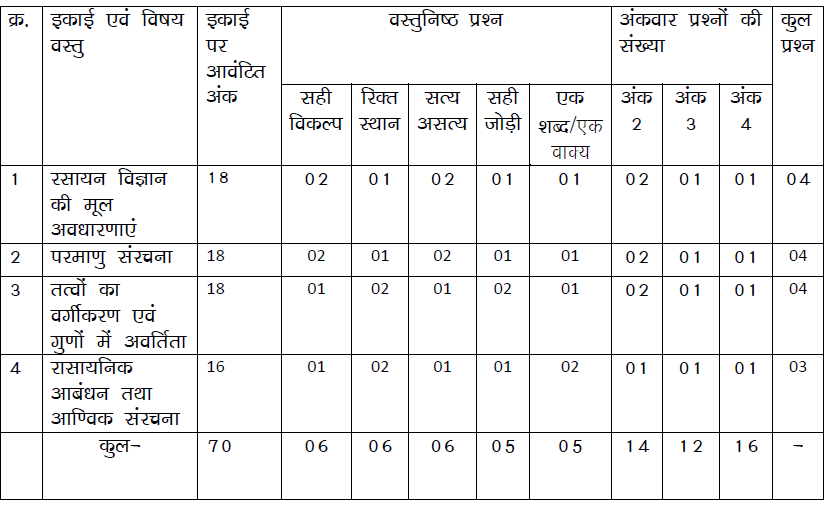
त्रैमासिक परीक्षा ब्लू प्रिंट
कक्षा-11वीं
विषय-रसायन विज्ञान
पूर्णांक-70 समय-3 घण्टे
निर्देश-
प्रश्न क्रमांक 01 से 05 तक वस्तुनिष्ठ प्रश्न होंगे कुल अंक 28
वस्तुनिष्ठ प्रश्नों को छोड़कर सभी प्रश्नों में आंतरिक विकल्प का प्रावधान होगा। यह विकल्प समान इकाई/उपइकाई से तथा समान कठिनाई स्तर वाले होंगे। इन प्रश्नों की उत्तर सीमा निम्नानुसार होगी –
अतिलघुउत्तरीय प्रश्न 02 अंक लगभग 20 से 30 शब्द
लघुउत्तरीय प्रश्न 03 अंक लगभग 40 से 50 शब्द
विश्लेषणात्मक प्रश्न 04 अंक लगभग 50 से 100 शब्द
इकाई-1 रसायन विज्ञान की मूल भूत अवधारणाएँ
प्रश्न 1: सही विकल्प चुनकर उत्तर लिखिए
- जल का मोलर द्रव्यमान होता है – (अ) 14 (ब) 18 (स) 44 (द) 10
- शुद्ध जल की मोलरता है – (अ) 18 (ब) 50 (स) 55 (द) 100
- CO2 का अणुभार है – (अ) 88 (ब) 44 (स) 18 (द) 38
- CO2 का मोलर द्रव्यमान है – (अ) 88 (ब) 44 (स) 18 (द) 38
- CH4 का मोलर द्रव्यमान है – (अ) 88 (ब) 44 (स) 18 (द) 16
- सोडियम सल्फेट (Na2SO4) में सोडियम का द्रव्यमान प्रतिशत 32.39% सल्फर का द्रव्यमान 22.54% है तो ऑक्सीजन का द्रव्यमान प्रतिशत होगा – (अ) 54.93% (ब) 10% (स) 50% (द) 45.07%
- एक मोल कार्बन को हवा में जलाया जाता है तो कितने ग्राम कार्बन डाई-ऑक्साइड प्राप्त होगी? (अ) 22 ग्राम (ब) 11 ग्राम (स) 44 ग्राम (द) 100 ग्राम
- एथेन के 3 मोलो में कार्बन के कितने मोल उपस्थित रहेंगे – (अ) 2 (ब) 3 (स) 6 (द) 4
- S.T.P पर 22.4 लीटर CO2 का द्रव्यमान होगा – (अ) 11 ग्राम (ब) 22 ग्राम (स) 44 ग्राम (द) 22.4 ग्राम
- 1.6 ग्राम मीथेन (CH4) के पूर्ण दहन से उत्पन्न CO2 की मात्रा होगी – (अ) 4.4 ग्राम (ब) 8.8 ग्राम (स) 44 ग्राम (द) 8.8 ग्राम
रिक्त स्थानों की पूर्ति कीजिए
(1) सामान्य ताप एवं दाब पर गैस के एक मोल अणुओं का आयतन ——— होता है।
(2) विलयन की सांद्रता व्यक्त करने कि वह विधि जो तापमान परिवर्तन से प्रभावित होती है ——— कहलाती है।
(3) ‘केमिस्ट्री’ शब्द की उत्पत्ति ———- शब्द से हुई जिसका अर्थ रासायनिक क्रिया होता है।
(4) जब प्रेक्षित मान व वास्तविक मान में अंतर बहुत कम होता है तो इसे ———— कहते हैं।
(5) किसी तत्व का वह सूक्ष्मतम कण जो रासायनिक अभिक्रिया में भाग लेता है किन्तु स्वतंत्र अवस्था में नहीं रह सकता _———— कहलाता है।
सत्य / असत्य लिखिए –
- द्रव्यमान व भार में अन्तर होता है।
- एवोगेड्रो नियम का उपयोग अणु की परमाणवीयता (Atomicity) ज्ञात करने में किया जाता है।
- जब सभी संख्याएँ पूर्णांक हो तो सार्थक अंकों की गणना का नियम प्रयुक्त नहीं होगा।
- वह अभिकर्मक जो रसासीकरण गणना के आधार पर कम होता है, सीमान्तक अभिकर्मक कहलाता है।
- भारानुसार प्रतिशत व प्रतिशत संघटन दोनों एक ही है।
एक शब्द / एक वाक्य में उत्तर दीजिए –
- समान ताप एवं समान दाब पर समस्त गैसों के समान आयतन में अणुओं की संख्या समान होती है यह नियम कहलाता है।
- 4 मोल CH4 का भार लिखिए।
- आण्विक सूत्र को मूलानुपाती सूत्र में कैसे प्राप्त करेंगे?
- स्टाइकियोमीट्री को एक वाक्य में समझाइये।
- वैज्ञानिक संकेतन को किस प्रकार व्यक्त करेंगे।
2 अंक वाले प्रश्न-
प्र.1 सार्थक अंको से आप क्या समझते है?
प्र.2 निम्न आंकड़ो को तीन सार्थक अंको तक निकटित कीजिए।
(i) 0.0025
(ii) 126000
प्र.3 पेयजल के नमूने में क्लोरोफॉर्म, जो कैंसरजन्य है, से अत्यधिक संदूषित पाया गया। संदूषण का स्तर 15 ppm था।
(i) क्लोरोफार्म का रासायनिक सूत्र लिखिए।
(ii) संदूषण का स्तर द्रव्यमान प्रतिशत में बताइये।
प्र.4 SI मात्रक का क्या अभिप्राय है? द्रव्यमान का SI मात्रक लिखिए।
प्र.5 निम्नलिखित को वैज्ञानिक संकेतन में लिखिए:
(i) 0.0048
(ii) 234000
3 अंक वाले प्रश्न –
प्र.1 निम्नलिखित के लिए मोलर द्रव्यमान का परिकलन कीजिए: (i) H2O (ii) CO2 (iii) CH4
प्र.2 आयरन के ऑक्साइड का आण्विक सूत्र ज्ञात कीजिए जिसमें आयरन तथा आक्सीजन का द्रव्यमान प्रतिशत क्रमशः: 69.9% एवं 30.1% है। Fe=55.85amu,O=16.00amu
प्र.3 गुणित अनुपात का नियम उदाहरण द्वारा समझाइये।
4 अंक वाले प्रश्न –
प्र.1 एथेन (C2H6) के तीन मोलो में निम्नलिखित का परिकलन कीजिए: (i) कार्बन परमाणुओं के मोलो की संख्या (ii) हाईड्रोजन परमाणुओं के मोलो की संख्या (iii) एथेन के अणुओं की संख्या
प्र.2 100 gm कॉपर सल्फेट से कितना कॉपर प्राप्त किया जा सकता है?
प्र.3 डॉल्टन का परमाणु सिद्धांत लिखते हुए इस सिद्धांत की दो प्रमुख कमियाँ लिखिए।
सही जोड़ी बनाइये-
निम्नलिखित रासायनिक समीकरण की सही जोड़ी बनाइये-
Part 1: Reactants
- 1.

- 2.

- 3.

- 4.

- 5.

Part 2: Products
- (a)

- (b)

- (c)

- (d)
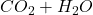
- (e)

इकाई-2 परमाणु संरचना
बहुविकल्पीय प्रश्न –
- सोडियम आयन (
 ) में इलेक्ट्रॉनों की संख्या है।
) में इलेक्ट्रॉनों की संख्या है।
(a) 11
(b) 12
(c) 10
(d) 23
- समस्थानिकों में संख्या समान होती है।
(a) प्रोटॉन
(b) न्यूट्रॉन
(c) प्रोटॉन तथा न्यूट्रॉन
(d) न्यूक्लिऑन
 आयन में इलेक्ट्रॉनों की संख्या होगी।
आयन में इलेक्ट्रॉनों की संख्या होगी।
(a) 19
(b) 18
(c) 17
(d) 20
 में न्यूट्रॉनों की संख्या है।
में न्यूट्रॉनों की संख्या है।
(a) 35
(b) 115
(c) 80
(d) 45
- एक तत्व के लिये उपकोश
 का मान 2 है इसमें कुल इलेक्ट्रॉन संख्या होगी।
का मान 2 है इसमें कुल इलेक्ट्रॉन संख्या होगी।
(a) 2
(b) 10
(c) 6
(d) 14
- निम्नलिखित में से कौन सी द्रव तरंगों की तरंगदैर्ध्य सबसे कम होती है जबकि वे समान गति से गमन कर रही हो?
(a) इलेक्ट्रॉन
(b) अल्फा कण
(c) न्यूट्रॉन
(d) प्रोटॉन
रिक्त स्थानों की पूर्ति कीजिए-
1. एक इलेक्ट्रॉन के लिये ![]() का मान
का मान ![]() है, तो इलेक्ट्रॉन ________ कक्ष में है।
है, तो इलेक्ट्रॉन ________ कक्ष में है।
2. जिस कक्षक के लिये ![]() एवं
एवं ![]() होगा उसे ________ से प्रदर्शित करेंगे।
होगा उसे ________ से प्रदर्शित करेंगे।
3. आवृत्ति के बढ़ते हुए क्रम में निम्न प्रकार से विकिरण होते हैं, रिक्त स्थान में उचित विकिरण का नाम लिखिए-
एफ एम रेडियो विकिरण < माइक्रोवेव ओवन < क्रमणि प्रकाश < ________ किरणों < कॉस्मिक किरणें।
4. यदि किसी परमाणु में ![]() का मान 4 है तो कुल इलेक्ट्रॉनों की संख्या ________ होगी।
का मान 4 है तो कुल इलेक्ट्रॉनों की संख्या ________ होगी।
5. संकरण के पश्चात प्राप्त ऑर्बिटल की ________ एवं ________ समान होती है।
सत्य / असत्य
1. किसी उपकोश के सभी कक्षकों में इलेक्ट्रॉनों का युग्मन तब तक नहीं होता जब तक कि उस उपकोश के सभी कक्षकों में एक-एक इलेक्ट्रॉन प्रविष्ट न हो जाए। (________)
2. दे-ब्रोग्ली का समीकरण सिर्फ गतिशील कण के लिये है। (________)
3. एक उपकक्ष में अधिकतम 6: इलेक्ट्रॉन आ सकते हैं। (________)
4. नाभिक में न्यूट्रॉन तथा प्रोटॉन पाए जाते हैं। (________)
5. कक्षक एवं कक्ष में कोई अंतर नहीं होता। (________)
सही जोड़ी बनाइये-
मैक्स प्लांक
रदर फोर्ड
हुण्ड
द-ब्रोग्ली समीकरण
पाउली
(a) λ=h/mc
(b) बहुलता का नियम
(c) क्वाटंम सिद्धांत
(d) अपवर्जन सिद्धांत
(e) नाभिक
एक शब्द/वाक्य में उत्तर-
- समान परमाणु क्रमांक परन्तु भिन्न द्रव्यमान अंक वाले परमाणु क्या कहलाते है?
- परमाणु में किसी इलेक्ट्राॅन की सही स्थिति दर्शाने वाली संरचना क्या कहलाती है?
- हाइड्रोजन परमाणु स्पेक्ट्रम की द्वितीय श्रृंखला क्या कहलाती है?
- हाइजेनबर्ग का अनिश्चितता का सिद्धांत क्या है?
- उच्चतम तरंगदैर्ध वाले विकिरण का नाम लिखिए।
- किस कक्षक में दिशात्मक प्रभाव नहीं होता है?
2 अंक वाले प्रश्न (कुल दो प्रश्न)
- किसी स्पीशीज में इलेक्ट्रोन, प्रोटोन तथा न्यूट्रोन की संख्या क्रमशः 18, 16 तथा 16 है। इसका उपयुक्त संकेत परमाण्वीय व आयनित अवस्था में लिखिए।
- एनोड किरणों के दो गुण लिखिए।
- कक्ष तथा कक्षक में दो अन्तर लिखिए।
- n+l नियम उदाहरण सहित लिखिए।
- हुण्ड का नियम लिखिए एवं कारण लिखिए कि हुण्ड के नियम को बहुलता का नियम किस कारण से कहते है?
3 अंक वाले प्रश्न – (कुल एक प्रश्न)
- हाइड्रोजन के समस्थानिकों के नाम एवं संरचनाए बनाते हुये इलेक्ट्रान, प्रोटोन, न्यूट्रॉन की संख्या लिखिए।
- इलेक्ट्राॅन की कण एवं तरंग प्रकृति को संक्षेप में समझाइए।
- रदरफोर्ड के α प्रकीर्णन प्रयोग के निष्कर्ष लिखिए।
- परमाणु संख्या पूर्णांक में होती है जबकि परमाणु द्रव्यमान पूर्णांक में नहीं भी हो सकते, कारण बताइये।
- ऑफबाऊ का नियम एक मुख्य उपयोग लिखते हुये ऑफबाऊ के नियम को चित्र द्वारा समझाइये।
4 अंक वाले प्रश्न – (कुल एक प्रश्न)
- क्वाटंम संख्या से आप क्या समझते हो? चारों क्वाटंम संख्याओं को समझाइये।
- परमाणु उदासीन क्यों होता है?
- Al तथा Si में 3p कक्षक में अयुग्मित इलेकट्रोन होते हैं। कौन से तत्व का इलेक्ट्राॅन नाभिक से अधिक प्रभावी नाभिकीय आवेश अनुभव करेगा?
- पाउली का अपवर्जन सिद्धांत एवं इसके महत्व को समझाइये।
- हाइड्रोजन स्पेक्ट्रम की चारों श्रेणियों का नाम लिखते हुये प्राप्त स्पेक्ट्रम का चित्र बनाइये।
इकाई-3 तत्वों का वर्गीकरण और गुणधर्मों में आवर्तिता
1 अंक वाले प्रश्न –
- बहुविकल्पीय
- एक तत्व का परमाणु क्रमांक 11 है, इसके ऑक्साइड की प्रकृति होगी- (a) अम्लीय (b) क्षारीय (c) उभयधर्मी (d) उदासीन
- B, C, N और O की इलेक्ट्राॅन बंधुता का क्रम है- (a) O > C > N > B (b) B > N > C > O (c) O > C > B > N (d) O > B > C > N
- आवर्त सारणी के किसी वर्ग में नीचे की ओर जाने में कौन-सा गुण नहीं बदलता है- (a) परमाणु आकार (b) घनत्व (c) संयोजक इलेक्ट्राॅन (d) धात्विक गुण
- लीथियम, मैग्रीशियम से रासायनिक व्यवहार में समानता प्रदर्शित करता है, क्योंकि- (a) समान आकार, समान ऋणविद्युतता और कम ध्रुवण क्षमता (b) समान आकार, अधिक ऋणविद्युतता और समान ध्रुवण क्षमता (c) समान आकार, समान ऋणविद्युतता और समान उच्च ध्रुवणक्षमता (d) इनमे से कोई नहीं
- निम्न में से किन तत्वों के युग्म में उनकी बाहरी कोश में उपस्थित इलेक्ट्रॉनों की संख्या बराबर होती है- (a) N, O (b) Na, Ca (c) As, Bi (d) Pb, Sb
- वर्ग में ऊपर से नीचे जाने पर कौन सा गुण सदैव बढेगा? (a) परमाण्वीय त्रिज्या (b) आयनन विभव (c) इलेक्ट्राॅन बंधुता (d)विद्युत ऋणता
- किसी तत्व के दिधनायन का विन्यास 2, 8, 14 हो तो, उसका परमाणु क्रमांक होगा- (a) 26 (b) 24 (c) 25 (d) 28
- एक वर्ग में ऊपर से नीचे जाने पर- (a) विद्युत ऋणता बढ़ती है (b) अपचायक सामर्थ्य बढ़ती है (c) ऑक्सीकारक सामर्थ्य बढ़ता है (d) आयनन विभव बढ़ता है
- इलेक्ट्राॅन बंधुता सर्वाधिक किसकी होगी? (a) F (b) Cl (c) Br (d) I
2. रिक्त स्थानों की पूर्ति कीजिए
- ऑक्सीजन की परमाण्विक त्रिज्या नाइट्रोजन से ________ होती है।
- जब किसी गैसीय परमाणु पर एक इलेक्ट्राॅन जोड़ा जाता है, तो निकलने वाली ऊर्जा को ________ कहते हैं।
- Mn ________ तत्व का उदाहरण है।
- बोराॅन विकर्णतः ________ से सम्बंधित है।
- न्यूनतम गलनांक वाली धातु ________ है।
- आवर्त तालिका में अधातु ________ ओर स्थित है।
3. निम्नलिखित प्रश्नों का एक शब्द / वाक्य में उत्तर दीजिये
- इलेक्ट्राॅन ग्रहण एन्थैल्पी को किसमें मापा जाता है?
- समूह में ऊपर से नीचे जाने पर परमाणु त्रिज्या पर क्या प्रभाव पड़ेगा?
- आवर्त में बाएँ से दाएँ जाने पर आयनन विभव पर क्या प्रभाव पड़ेगा?
4. उचित संबंध जोड़िए
[A]
‘अ’
- 1. परमाणु भार पर आधारित आवर्त सारणी
- 2. परमाणु संख्या पर आधारित आवर्त सारणी
- 3. विद्युत ऋणात्मकता = 4
- 4. सामान्य इलेक्ट्रॉनिक विन्यास =

- 5.

‘ब’
- (a) बोर की आवर्त सारणी
- (b) फ्लुओरीन
- (c) मेन्डलीफ आवर्त सारणी
- (d) समइलेक्ट्रॉनिक आयन
- (e) संक्रमण तत्व
[B]
‘अ’
- 1. न्यूलैण्ड ने दिया
- 2. मेंडलीव की आवर्त सारणी में
- 3. आधुनिक आवर्त सारणी में
- 4. वर्ग-1
- 5. वर्ग-2
‘ब’
- (a) क्षारीय मृदा धातुएँ
- (b) 7 क्षैतिज खाने व 18 ऊर्ध्वाधर खाने
- (c) अष्टक नियम
- (d) 7 क्षैतिज खाने व 9 ऊर्ध्वाधर खाने
- (e) क्षारीय धातुएँ
5. 2 अंक वाले प्रश्न-
1. एक ही वर्ग में उपस्थित तत्वों के भौतिक और रासायनिक गुणधर्म समान क्यों होते हैं?
2. धनायन अपने जनक परमाणुओं से छोटे क्यों होते हैं और ऋणायनों की त्रिज्या उनके जनक परमाणुओं की त्रिज्या से अधिक क्यों होती है? व्याख्या कीजिए।
3. इलेक्ट्रॉन लब्धि एंथैल्पी और इलेक्ट्रॉन ऋणात्मकता में क्या मूल अंतर है?
6. 3 अंक वाले प्रश्न –
दीर्घ आवर्त तालिका पुरानी आवर्त तालिका से किस प्रकार बेहतर है?
d-ब्लॉक तत्वों के सामान्य लक्षण क्या है?
आवर्त तालिका के आवर्त में बाये से दायें जाने पर निम्न गुणों में क्या परिवर्तन होते हैं-
(i) परमाण्विक त्रिज्या, (ii) आयनन ऊर्जा, (iii) इलेक्ट्राॅन बंधुता।
- 4 अंक वाले प्रश्न-
सोडियम आयन सोडियम से आकार में छोटा किन्तु फ्लुओराइड आयन फ्लुओरीन से आकार में बड़ा होता है, क्यों?
‘टिपिकल’ तत्वों से क्या समझते हैं? इनका इलेक्ट्राॅनिक विन्यास क्या है?
निम्नलिखित को समझाइये-
(i) आयनन विभव, (ii) इलेक्ट्राॅन बंधुता।
इकाई-4 रासायनिक आबंधन तथा आण्विक संरचना
1 अंक वाले प्रश्न
- बहुविकल्पीय प्रश्न
- निम्न में से किसमें सर्वाधिक सहसंयोजी गुण होते हैं?
(a) ![]()
(b) ![]()
(c) ![]()
(d) ![]()
- MO सिद्धान्तानुसार
 आयन में प्रतिबंधित इलेक्ट्रॉन युग्म की संख्या है-
आयन में प्रतिबंधित इलेक्ट्रॉन युग्म की संख्या है-
(a) 4
(b) 3
(c) 2
(d) 5
- धातु M का इलेक्ट्रॉनिक विन्यास
 है। इसके ऑक्साइड का सूत्र होगा-
है। इसके ऑक्साइड का सूत्र होगा-
(a) ![]()
(b) ![]()
(c) ![]()
(d) ![]()
- निम्न में से कौन-सा अणु अरेखीय है-
(a) ![]()
(b) ![]()
(c) ![]()
(d) तीनों सही
- निम्न में से कौन-सा अनुचुम्बकीय नहीं है?
(a) ![]()
(b) ![]()
(c) ![]()
(d) ![]()
- निम्न में से किस स्पीशीज में अयुग्मित इलेक्ट्रॉन होंगे-
(a) ![]()
(b) ![]()
(c) ![]()
(d) ![]()
- निम्न में से किसका द्विध्रुव आघूर्ण शून्य है-
(a) ![]()
(b) ![]()
(c) ![]()
(d) ![]()
- बंध कोण बढ़ने के साथ द्विध्रुव आघूर्ण का मान-
(a) बढ़ता है
(b) घटता है
(c) अपरिवर्तित रहता है
(d) घट भी सकता है या बढ़ भी सकता है
- निम्न में से किस अणु में सभी बंध समान नहीं होते हैं-
(a) ![]()
(b) ![]()
(c) ![]()
(d) ![]()
- निम्न में से कौन ध्रुवीय अणु है?
(a) ![]()
(b) ![]()
(c) ![]()
(d) ![]()
2. रिक्त स्थानों की पूर्ति कीजिए-
- सभी रासायनिक बन्धों का स्थायित्व ………… के मध्य आकर्षण बढ़ने से होता है।
- सहसंयोजक यौगिकों का गलनांक सामान्यतः ………… होता है।
- नाइट्रोजन अणु में ………… π-बन्ध होते हैं।
- कार्बन मोनोक्साइड में कार्बन की सहसंयोजकता ………… है।
- NH3 अणु की आकृति ………… है।
- आयनिक यौगिक सामान्यतः जल में ………… होते हैं।
3. उचित संबंध जोड़िये-
[A]
- आयनिक बन्ध
- सहसंयोजी बन्ध
- उप-सहसंयोजक बन्ध
- HF
- HCl
[B] (a) इलेक्ट्रॉनों का साझा (b) ध्रुव है (c) गैस है (d) इलेक्ट्रॉनों का स्थानान्तरण (e) इलेक्ट्राॅन युग्म का दान।
- निम्नलिखित प्रश्नों का एक शब्द / वाक्य में उत्तर दीजिए-
- परमाणु द्वारा साझे के इलेक्ट्रॉन युग्म को अपनी ओर आकर्षित करने की क्षमता कहलाती है।
- बेंजीन के अणु में कितने सिग्मा बंध और कितने पाई बंध उपस्थित हैं?
- बंध लंबाई को नापने की इकाई लिखिए।
सत्य / असत्य
 अणु में
अणु में  संकरण पाया जाता है।
संकरण पाया जाता है।- नाइट्रोजन अणु में बंधन कम का मान 3 (तीन) होता है।
 संकरण की ज्यामिति अष्टफलकीय होती है।
संकरण की ज्यामिति अष्टफलकीय होती है।
02 अंक वाले प्रश्न-
- यद्यपि
 तथा
तथा  दोनों अणुओं की ज्यामिति विकृत चतुष्फलकीय होती है, तथापि जल में आबंध कोण अमोनिया की अपेक्षा कम होता है। विवेचना कीजिए।
दोनों अणुओं की ज्यामिति विकृत चतुष्फलकीय होती है, तथापि जल में आबंध कोण अमोनिया की अपेक्षा कम होता है। विवेचना कीजिए। - आबंध प्रबलता को आबंध-कोटि से जोड़कर परिभाषित कीजिये।
 तथा
तथा  में किस अणु का द्विध्रुव-आघूर्ण अधिक है और क्यों?
में किस अणु का द्विध्रुव-आघूर्ण अधिक है और क्यों?
03 अंक वाले प्रश्न-
- निम्नलिखित अणुओं में सिग्मा तथा पाई (
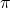 ) आबंधों की कुल संख्या कितनी है? (क)
) आबंधों की कुल संख्या कितनी है? (क)  (ख)
(ख) 
 और
और  में किसमें सहसंयोजी गुण अधिक होगा और क्यों?
में किसमें सहसंयोजी गुण अधिक होगा और क्यों? विलयन
विलयन  विलयन के साथ सफेद अवक्षेप देता है किन्तु
विलयन के साथ सफेद अवक्षेप देता है किन्तु  नहीं, क्यों?
नहीं, क्यों?
दीर्घ उत्तरीय प्रश्न- 04 अंक
- VSEPR सिद्धान्ता का उदाहरण देकर समझाइए।
- आयनिक बंध क्या है? इसके बनने के लिए अनुकूल परिस्थितियां समझाइए।
- जालक ऊर्जा क्या है? यह किन कारकों पर निर्भर करती है? आयनिक यौगिकों के स्थायित्व को यह कैसे समझाती है?