mP Board 12th Chemistry Quarterly Exam 2025-26 Question Bank :
रसायन विज्ञान ब्लूप्रिंट (तालिका)
| स. क्र. | इकाई एवं विषय वस्तु | इकाई पर आबंटित अंक | वस्तुनिष्ठ प्रश्न (1 अंक) | प्रश्नों की संख्या (2 अंक) | प्रश्नों की संख्या (3 अंक) | प्रश्नों की संख्या (4 अंक) | कुल प्रश्न |
|---|---|---|---|---|---|---|---|
| 1 | विलयन | 14 | 05 | 01 | 01 | 01 | 03 |
| 2 | विद्युत रसायन | 18 | 06 | 02 | – | 02 | 04 |
| 3 | d व f-ब्लॉक के तत्व | 14 | 05 | 01 | 01 | 01 | 03 |
| 4 | उपसहसंयोजन रसायन | 12 | 05 | 02 | 01 | – | 03 |
| 5 | हैलो ऐल्केन व हैलो ऐरीन | 12 | 07 | 01 | 01 | – | 02 |
| कुल योग | 70 | 28 | 14 | 14 | 12 | 16 |
इकाई – 1 विलयन (07)
Q.1. सही विकल्प चुनकर लिखिए –
- जर्मन सिल्वर मिश्रण होता है- (A) Cu + Zn (B) Cu + Zn + Ni (C) Cu + Sn (D) Zn + Sn
- दो या दो से अधिक अवयवों का समांगी मिश्रण है- (A) विलयन (B) द्रव विलय (C) द्रव विलायक (D) विलायक
- पीतल है – (A) ठोस विलयन (B) द्रव विलयन (C) गैस विलयन (D) कोलाइडी विलयन
- गैसों की द्रव में विलेयता का नियम दिया था- (A) हेनरी ने (B) वाण्ट हॉफ ने (C) बर्कले ने (D) बॉयल ने
- एथेनॉल जल में घुलनशील है इसका मुख्य उदाहरण है (A) गैसीय विलयन (B) कोलाइडी विलयन (C) द्रव विलयन (D) ठोस विलयन
- यदि 5.85gm NaCl को 250gm जल में घोला जाता है तो विलयन की मोलरता होगी- (A) 0.4 (B) 0.5 (C) 1.4 (D) 2.3M
- एक मिलियन विलयन में उपस्थित विलेय के ग्रामों की संख्या कहलाती है- (A) M (B) m (C) ppm (D) मोल प्रभाज
बहुविकल्पीय प्रश्न
- यदि
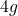 NaOH,
NaOH, 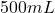 विलयन में उपस्थित है, तो विलयन की मोललता होगी –
विलयन में उपस्थित है, तो विलयन की मोललता होगी – - उच्चतम क्वथन स्थिर क्वाथी मिश्रण का मुख्य उदाहरण है-
- जल के लिए मोलल क्वथनांक उन्नयन स्थिरांक का मान है-
(A) ![]() (B)
(B) ![]() (C)
(C) ![]() (D)
(D) ![]()
(A) ![]() (B)
(B) ![]() (C)
(C) ![]() (D)
(D) ![]()
(A) ![]() (B)
(B) ![]() (C)
(C) ![]() (D)
(D) ![]()
प्रश्न 4. सही जोड़ी मिलाइए –
| ‘A’ | ‘B’ |
|---|---|
| 1. मोलरता | (a) |
| 2. हिमांक में अवनमन | (b) |
| 3. वांट हॉफ गुणांक | (c) मोलों की संख्या |
| 4. प्रदूषण | (d) |
| 5. एस्पिरिन | (e) ppm |
| ‘A’ | ‘B’ |
|---|---|
| 1. |
(a) |
| 2. ऋणात्मक विचलन | (b) |
| 3. हेनरी नियम | (c) एसीटोन + क्लोरोफॉर्म |
| 4. गैस का द्रव में विलयन | (d) धुआँ |
| 5. ठोस का गैस में विलयन | (e) सोडावाटर |
4 Marks
- मोलरता व मोललता में चार अंतर लिखिए।
- मोलल हिमांक अवनमन स्थिरांक की परिभाषा एवं विलेय के अणुभार से इसका संबंध स्थापित कीजिए।
- राउल्ट का नियम एवं इसके आधार पर विलेय के मोलर द्रव्यमान निर्धारण के लिए गणितीय व्यंजक की व्युत्पत्ति कीजिए।
- मोलल क्वथनांक उन्नयन स्थिरांक की परिभाषा एवं विलेय के अणुभार से इसका संबंध स्थापित कीजिए।
- धनात्मक एवं ऋणात्मक विचलन दर्शाने वाले अनादर्श विलयन में चार अंतर लिखिए।
- यदि N2 गैस को 293K पर जल में से प्रवाहित किया जाए तो एक लीटर जल में कितने मिलीमोल N2 गैस विलेय होगी? N2 का आंशिक दाब 0.987bar है तथा 293K पर N2 के लिए KH का मान 76.48kbar है।
- बेंजीन का क्वथनांक 353.23K है। 1.80g अवाष्पशील विलेय को 90g C6H6 में घोलने पर विलयन का क्वथनांक बढ़कर 354.11K हो जाता है। विलेय के मोलर भार की गणना कीजिए। बेंजीन के लिए Kb का मान 2.53K kg mol−1 है।
Q.3. सत्य / असत्य –
- 1000 ग्राम विलायक में उपस्थित विलेय के मोलों की संख्या मोलरता कहलाती है।
- निश्चित ताप पर विलयन का परासरण दाब विलेय की मोलर सान्द्रण के समानुपाती होता है।
- ऐसे सभी गुणधर्म जो विलयन में उपस्थित कुल कणों की संख्या पर निर्भर करते हैं न कि विलेय कणों की प्रकृति पर ऐसे गुणों को अणुसंख्यक गुणधर्म कहते हैं।
- वह विलयन जो संघटन में बिना परिवर्तन के आसवित होता है स्थिरक्वाथी मिश्रण (एजोट्रॉप) कहलाता है।
- वे विलयन जिनमें विलेय की मात्रा अपेक्षाकृत अधिक होती है तनु विलयन कहलाते हैं।
- जल में उपस्थित फ्लुओराइड आयनों की एक पी.पी.एम. (ppm) मात्रा दंतक्षय को रोकती, किन्तु 1.5 पी.पी.एम. मात्रा दाँतों को कर्बुरित (पीलापन) होने का कारण होती है।
- ऐसा मोलर द्रव्यमान जो सामान्य मान की तुलना में निम्न या उच्च होता है असामान्य मोलर द्रव्यमान कहलाता है।
- सोडा-जल एवं शीतल पेयों में CO2 की विलेयता बढ़ाने के लिए बोतल को अधिक दाब पर बंद किया जाता है।
- साम्यावस्था में वाष्प प्रावस्था हमेशा उस अवयव की धनी होती है जो अधिक वाष्पशील होता है।
- विलयन जो एक निश्चित संघटन पर राउल्ट के नियम से अत्यधिक ऋणात्मक विचलन प्रदर्शित करते हैं, उच्चतम क्वथनांक की स्थिरक्वाथी बनाते हैं।
Q.5. एक वाक्य / शब्द में उत्तर दीजिए –
- किसी विलयन के 1000 ग्राम विलायक में उपस्थित विलेय के मोलों की संख्या कहलाती है –
- बिना संघटन में परिवर्तन के निश्चित ताप पर आसवित होने वाले विलयन क्या कहलाते हैं –
- परासरण दाब ज्ञात करने का सूत्र लिखो।
- आदर्श विलयन का एक उदाहरण लिखिए।
- विपरीत परासरण में अर्द्धपारगम्य झिल्ली किसकी बनी होती है।
- अणुसंख्यक गुणधर्म के प्रेक्षित मान एवं सैद्धांतिक मान के अनुपात को क्या कहा जाता है –
- एक ऐसे ठोस विलयन का उदाहरण दीजिए जिसमें विलेय कोई गैस हो।
- अर्द्धपारगम्य झिल्ली मुख्य रूप से किसकी बनी होती है।
- विलयन में विलेय की मात्रा कम होने पर विलयन कहलाता है।
- एक मिल्यिन विलयन में उपस्थित विलेय की मात्रा को क्या कहा जाता है –
2 Marks
- समपरासारी विलयन की परिभाषा लिखिए।
- 5gm NaOH, 450ml विलयन में घुला हुआ है तो विलयन की मोलरता ज्ञात कीजिए।
- हेनरी का नियम लिखो।
- प्रतिलोम परासरण की परिभाषा लिखो।
- 2.5gm एथेनोइक अम्ल के 75gm बेंजीन में विलयन की मोललता ज्ञात कीजिए।
- 4gm NaOH, 90gm जल में उपस्थित है तो विलेय के मोल प्रभाज की गणना करो।
- एक प्रोटीन के 200cm3 जलीय विलयन में 1.26g प्रोटीन है। 300K पर इस विलयन का परासरण दाब 2.57×10−3bar पाया गया। प्रोटीन के मोलर द्रव्यमान का परिकलन कीजिए।
इकाई – 2 विद्युत रसायन (09)
Q.1 सही विकल्प चुनकर लिखिए
- जब
 तथा
तथा  आयनों की सांद्रता इकाई होती है तो इस प्रकार की युक्ति को कहा जाता है-
आयनों की सांद्रता इकाई होती है तो इस प्रकार की युक्ति को कहा जाता है-
- (A) गैल्वेनिक सेल
- (B) ईंधन सेल
- (C) शुष्क सेल
- (D) Ni-Cd सेल
- प्रतिरोधकता (विशिष्ट प्रतिरोध) का प्रतिलोम कहलाता है-
- (A) मोलर चालकता
- (B) विशिष्ट चालकता
- (C) आयनिक चालकता
- (D) चालकता
- मोलर चालकता (आणविक) की इकाई है-
- (A) S

- (B)

- (C)

- (D)

- (A) S
- जंग का सही सूत्र है-
- (A)

- (B)

- (C)

- (D)

- (A)
- सेल स्थिरांक की इकाई है-
- (A)

- (B)

- (C)

- (D)

- (A)
 अभिक्रिया है-
अभिक्रिया है-
- (A) ऑक्सीकरण
- (B) अपचयन
- (C) विस्थापन
- (D) रेडॉक्स
- संचायक सेल में प्रयुक्त होने वाला पदार्थ है –
- (A) कॉपर
- (B) सिल्वर
- (C) लेड
- (D) सोडियम
- SHE के विभव का मान है-
- (A) 2.0 V
- (B) 1.5 V
- (C) 0.0V
- (D) 1.22V
- लोहे में जंग लगने कि क्रिया है –
- (A) बहुलीकरण
- (B) अपचयन
- (C) हाइड्रोजनीकरण
- (D) ऑक्सीकरण
Q.2. रिक्त स्थानों की पूर्ति कीजिए –
- मानक हाइड्रोजन इलेक्ट्रोड या नार्मल हाइड्रोजन इलेक्ट्रोड सेल का विभव ………………. होता है।
- लोहे पर जिंक धातु की परत चढ़ाना ………………. कहलाता है।
- सीसा संचायिका सेल में ………………. विद्युत अपघट्य का उपयोग किया जाता है।
- ऐसे पदार्थ जो जलीय विलयन में अत्यधिक आयनीत होते हैं ………………. कहलाते है।
- ………………. में ईंधन की रासायनिक ऊर्जा को विद्युत ऊर्जा में बदला जाता है।
- 1 मोल
 को Al में अपचयन के लिए ………………. फैराडे आवेश की आवश्यकता है।
को Al में अपचयन के लिए ………………. फैराडे आवेश की आवश्यकता है। - गलित
 से 20 gm Ca को प्राप्त करने के लिए ………………. फैराडे विद्युत की आवश्यकता है।
से 20 gm Ca को प्राप्त करने के लिए ………………. फैराडे विद्युत की आवश्यकता है।  ईंधन सेल की दक्षता लगभग ………………. है।
ईंधन सेल की दक्षता लगभग ………………. है।- 298K पर 0.20M KCl विलयन की चालकता 0.0248 S
 है तो इसकी मोलर चालकता ………………. होगी।
है तो इसकी मोलर चालकता ………………. होगी। - ऐसे गैल्वेनी सेलों को जिनमें हाइड्रोजन, मेथेन व मेथेनॉल आदि ईंधनों की दहन ऊर्जा को सीधे ही विद्युत ऊर्जा में परिवर्तित किया जाता है ………………. कहलाता है।
Q.3. सत्य / असत्य –
- सीसा संचायिका सेल की अनावेषित क्रिया
 है।
है। - किसी विलयन की विशिष्ट चालकता इसके एक घन सेमी. विलयन की चालकता होती है।
- किसी विलयन की आणविक चालकता, उसकी विशिष्ट चालकता एवं उसके आयतन के गुणनफल के बराबर होती है, जिसमें विद्युत अपघट्य का एक मोल घुला हो।
- 25°C व एक वायुमंडल दाब पर मोलर हाइड्रोजन आयन के सम्पर्क में हाइड्रोजन गैस, मानक हाइड्रोजन इलेक्ट्रोड का निर्माण करती है।
- अनन्त तनुता पर किसी विद्युत अपघट्य विलयन की आणविक चालकता का मान, अनन्त तनुताओं पर उसके दोनों आयनों की चालकताओं के योग के बराबर होता है यह कोलराउश नियम है।
 गैस प्रबलतम ऑक्सीकारक है एवं फ्लोराइड आयन दुर्बलतम अपचायक है।
गैस प्रबलतम ऑक्सीकारक है एवं फ्लोराइड आयन दुर्बलतम अपचायक है।- जब इलेक्ट्रॉन एक सिरे से प्रवेश करते है एवं दूसरे सिरे से निकल जाते है इसलिए धात्विक चालक का संघटन अपरिवर्तित रहता है।
- गैल्वेनी सेल की वह अर्द्ध सेल जिसमें ऑक्सीकरण होता एनोड कहलाती है एवं विलयन के सापेक्ष इसका विभव ऋणात्मक होता है।
- 1 मोल
 को
को  में बदलने के लिए 3 फैराडे आवेश की आवश्यकता होगी।
में बदलने के लिए 3 फैराडे आवेश की आवश्यकता होगी। - संक्षारण में धातु ऑक्सीजन को इलेक्ट्रॉन देकर ऑक्सीकृत हो जाती है एवं उनका ऑक्साइड बन जाता है।
Q. 4. सही जोड़ी मिलाइए –
| ‘A’ | ‘B’ |
| 1. 1 मोल | (a) सीसा संचायक सेल |
| 2. 1 मोल | (b) |
| 3. एक फैराडे | (c) ऑक्सीकरण (उपचयन) |
| 4. विद्युत रासायनिक सेल | (d) अपचयन |
| 5. कोलराउश नियम | (e) |
| 6. द्वितीयक सेल | (f) डेनियल सेल |
| 7. सेल स्थिरांक | (g) 96500 |
2 अंकीय प्रश्न:
- मानक हाइड्रोजन इलेक्ट्रोड विभव की परिभाषा लिखिए।
- फैराडे का प्रथम नियम लिखिए।
- जिंक के पात्र में कॉपर सल्फेट विलयन नहीं रखा जा सकता है। क्यों?
- प्रबल विद्युत अपघट्य की परिभाषा लिखिए।
- बैटरी की परिभाषा लिखिए।
- हाइड्रोजन को छोड़कर ईंधन सेल में प्रयुक्त होने वाले दो अन्य पदार्थों के नाम लिखिए।
- किसी विलयन की चालकता तनुता के साथ क्यों घटती है?
- एनोड किसे कहते हैं।
- अर्धचालक किसे कहते हैं।
 ,
,  एवं
एवं  के लिए
के लिए  क्रमश:
क्रमश:  ,
,  व
व  S
S  है,
है,  के लिए
के लिए  का मान ज्ञात कीजिए।
का मान ज्ञात कीजिए।
Q. 5. एक वाक्य / शब्द में उत्तर दीजिए –
- ऐसी अभिक्रिया जिसमें ऑक्सीकरण एवं अपचयन साथ-साथ हो वह अभिक्रिया क्या कहलाती है।
- ऐसी युक्ति जिसके द्वारा रासायनिक ऊर्जा को विद्युत ऊर्जा में बदला जाता है, क्या कहलाती है।
- किसी चालक का विभवान्तर उस चालक में बहने वाली विद्युत धारा के समानुपाती होता है, यह नियम किसने दिया था।
- क्या कॉपर सल्फेट विलयन को जिंक के बर्तन में रखा जा सकता है।
- प्रबल अपचायक का एक उदाहरण लिखिए।
- नम वायुमण्डल या रासायनिक अभिकर्मकों द्वारा धातुओं का धीरे-धीरे नष्ट होना क्या कहलाता है।
- किसी विलयन चालकता तनुता के साथ घटती है क्यों?
- गैल्वेनी सेल के दोनों इलेक्ट्रोडों के बीच विभवान्तर क्या कहलाता है।
- नम वायुमण्डल या रासायनिक अभिकर्मकों द्वारा धातुओं का धीरे-धीरे नष्ट होना क्या कहलाता है।
- सीसा संचायिका सेल की आवेशित होने वाली क्रिया लिखिए।
4 अंकीय प्रश्न:
- कोलराउश का नियम और इसके दो अनुप्रयोग लिखिए।
- मोलर चालकता तथा विशिष्ट चालकता कि परिभाषा, सूत्र, इकाई व इन पर तनुता का प्रभाव समझाइए।
- सीसा संचायिका सेल का सचित्र वर्णन करो एवं जब बैटरी उपयोग में होती है, तो इसमें होने वाली सेल अभिक्रियाएँ लिखिए।
 mol
mol  मेथेनोइक अम्ल की चालकता
मेथेनोइक अम्ल की चालकता  S
S  है, इसकी वियोजन मात्रा एवं वियोजन स्थिरांक का परिकलन कीजिए। दिया गया है
है, इसकी वियोजन मात्रा एवं वियोजन स्थिरांक का परिकलन कीजिए। दिया गया है  S
S  and
and  S
S  ।
।- विद्युत रासायनिक सेल (डेनियल सेल) की परिभाषा और इसका सचित्र वर्णन व सेल अभिक्रियाएँ लिखिए।
- निम्न को समझाइए –
- मानक हाइड्रोजन इलेक्ट्रोड विभव
- ईंधन सेल
- निम्न को हल कीजिए-
 K पर एक चालकता सेल जिसमें
K पर एक चालकता सेल जिसमें  M KCl विलयन है, का प्रतिरोध
M KCl विलयन है, का प्रतिरोध 
 है। यदि
है। यदि  M KCl विलयन की चालकता
M KCl विलयन की चालकता  K पर
K पर  S
S  पर हो तो सेल स्थिरांक क्या है?
पर हो तो सेल स्थिरांक क्या है? के विलयन को
के विलयन को  एम्पीयर की धारा से
एम्पीयर की धारा से 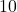 मिनट तक वैद्युतअपघटित किया गया। कैथोड पर निक्षेपित कॉपर का द्रव्यमान क्या होगा?
मिनट तक वैद्युतअपघटित किया गया। कैथोड पर निक्षेपित कॉपर का द्रव्यमान क्या होगा?
- संक्षारण की परिभाषा एवं संक्षारण का विद्युत रासायनिक सिद्धांत एवं बचाव के उपाय लिखिए।
- निम्नलिखित सेलों की
 K पर नर्न्स्ट समीकरण एवं emf लिखिए-
K पर नर्न्स्ट समीकरण एवं emf लिखिए-